жҒ©з»ҙиҫҫ®пјҲжҒ©жІғеҲ©еҚ•жҠ—жіЁе°„ж¶Іпјӣз ”еҸ‘д»ЈеҸ·пјҡKN035пјү* жҳҜеә·е®Ғжқ°з‘һиҮӘдё»з ”еҸ‘зҡ„PD-L1еҚ•еҹҹжҠ—дҪ“FcиһҚеҗҲиӣӢзҷҪпјҢжҳҜе…Ёзҗғ第дёҖдёӘдё”зӣ®еүҚе”ҜдёҖиҺ·жү№дёҠеёӮзҡ„зҡ®дёӢжіЁе°„PD-(L)1жҠ—дҪ“гҖӮеҹәдәҺе…¶зӢ¬зү№и®ҫи®ЎпјҢеңЁе®үе…ЁжҖ§гҖҒдҫҝеҲ©жҖ§е’Ңдҫқд»ҺжҖ§ж–№йқўе…·жңүдјҳеҠҝпјҢжӮЈиҖ…ж— йңҖиҝӣиЎҢйқҷи„үж»ҙжіЁпјҢеҗҢж—¶е…·жңүиҫғдҪҺзҡ„еҢ»з–—жҲҗжң¬гҖӮзӣ®еүҚжӯЈеңЁдёӯеӣҪгҖҒзҫҺеӣҪе’Ңж—Ҙжң¬ејҖеұ•еӨҡдёӘиӮҝзҳӨйҖӮеә”з—Үзҡ„дёҙеәҠз ”з©¶пјҢеӨҡдёӘйҖӮеә”з—Үе·Іиҝӣе…ҘжіЁеҶҢ/в…ўжңҹдёҙеәҠгҖӮжҒ©з»ҙиҫҫ®пјҲжҒ©жІғеҲ©еҚ•жҠ—жіЁе°„ж¶Іпјүе·Іиў«зҫҺеӣҪFDAжҺҲдәҲжҷҡжңҹиғҶйҒ“зҷҢеӯӨе„ҝиҚҜиө„ж јгҖҒиҪҜз»„з»ҮиӮүзҳӨеӯӨе„ҝиҚҜиө„ж јгҖӮ2021е№ҙ11жңҲпјҢжҒ©з»ҙиҫҫ®еңЁдёӯеӣҪиҺ·жү№дёҠеёӮпјҢйҖӮз”ЁдәҺдёҚеҸҜеҲҮйҷӨжҲ–иҪ¬з§»жҖ§еҫ®еҚ«жҳҹй«ҳеәҰдёҚзЁіе®ҡпјҲMSI-HпјүжҲ–й”ҷй…Қдҝ®еӨҚеҹәеӣ зјәйҷ·еһӢпјҲdMMRпјүзҡ„жҲҗдәәжҷҡжңҹе®һдҪ“зҳӨжӮЈиҖ…зҡ„жІ»з–—гҖӮ
KN035 : жҷ¶дҪ“з»“жһ„
д»ҘеҫҖеёӮеңәдёҠзҡ„PD-(L)1жІ»з–—йңҖиҰҒйў‘з№ҒиҝӣиЎҢйқҷи„үж»ҙжіЁпјҢж—ўдёҚиғҪж»Ўи¶іжӮЈиҖ…з”ЁиҚҜзҡ„дҫҝжҚ·жҖ§йңҖжұӮпјҢд№ҹе°ҶеҪұе“ҚжӮЈиҖ…дҪҝз”ЁиҚҜзү©зҡ„дҫқд»ҺжҖ§гҖӮи¶ҠжқҘи¶ҠеӨҡзҡ„иӮҝзҳӨжӮЈиҖ…жңҹеҫ…жӣҙеҠ дҫҝжҚ·зҡ„PD-(L)1з–—жі•:
жҒ©з»ҙиҫҫ®пјҲжҒ©жІғеҲ©еҚ•жҠ—жіЁе°„ж¶Іпјӣз ”еҸ‘д»ЈеҸ·пјҡKN035пјүжҳҜе…ЁзҗғйҰ–дёӘдёҠеёӮзҡ„зҡ®дёӢжіЁе°„PD-L1жҠ‘еҲ¶еүӮпјҢжӮЈиҖ…ж— йңҖиҝӣиЎҢйқҷи„үж»ҙжіЁе°ұеҸҜд»ҘеңЁ30з§’еҶ…е®ҢжҲҗз»ҷиҚҜпјҢеӨ§еӨ§зј©зҹӯдәҶз»ҷиҚҜж—¶й—ҙпјҢе…·жңүеұ…家иҮӘдё»з»ҷиҚҜзҡ„жҪңеҠӣпјҢд»ҺиҖҢжӣҙеҘҪең°ж”№е–„жӮЈиҖ…зҡ„з”ҹжҙ»иҙЁйҮҸгҖӮ
ASCO 2020 posterпјҡжҒ©жІғеҲ©еҚ•жҠ—пјҲKN035пјүз”ЁдәҺй”ҷй…Қдҝ®еӨҚзјәйҷ·зҡ„жҷҡжңҹиӮҝзҳӨзҡ„дёҙеәҠж•°жҚ®
ASCO 2019 posterпјҡKN035еңЁж—Ҙжң¬жҷҡжңҹе®һдҪ“зҳӨжӮЈиҖ…дёӯзҡ„е®үе…ЁжҖ§е’ҢиҚҜд»ЈеҠЁеҠӣеӯҰз ”з©¶
ASCO 2019 posterпјҡKN035еңЁдёӯеӣҪжҷҡжңҹе®һдҪ“зҳӨжӮЈиҖ…дёӯзҡ„в… жңҹдёҙеәҠз ”з©¶
ESMO 2018 posterпјҡKN035пјҲдёҖз§Қж–°еһӢжҠ—PD-L1иһҚеҗҲжҠ—дҪ“пјүеңЁзҫҺеӣҪжҷҡжңҹе®һдҪ“зҳӨжӮЈиҖ…дёӯзҡ„в… жңҹдёҙеәҠз ”з©¶
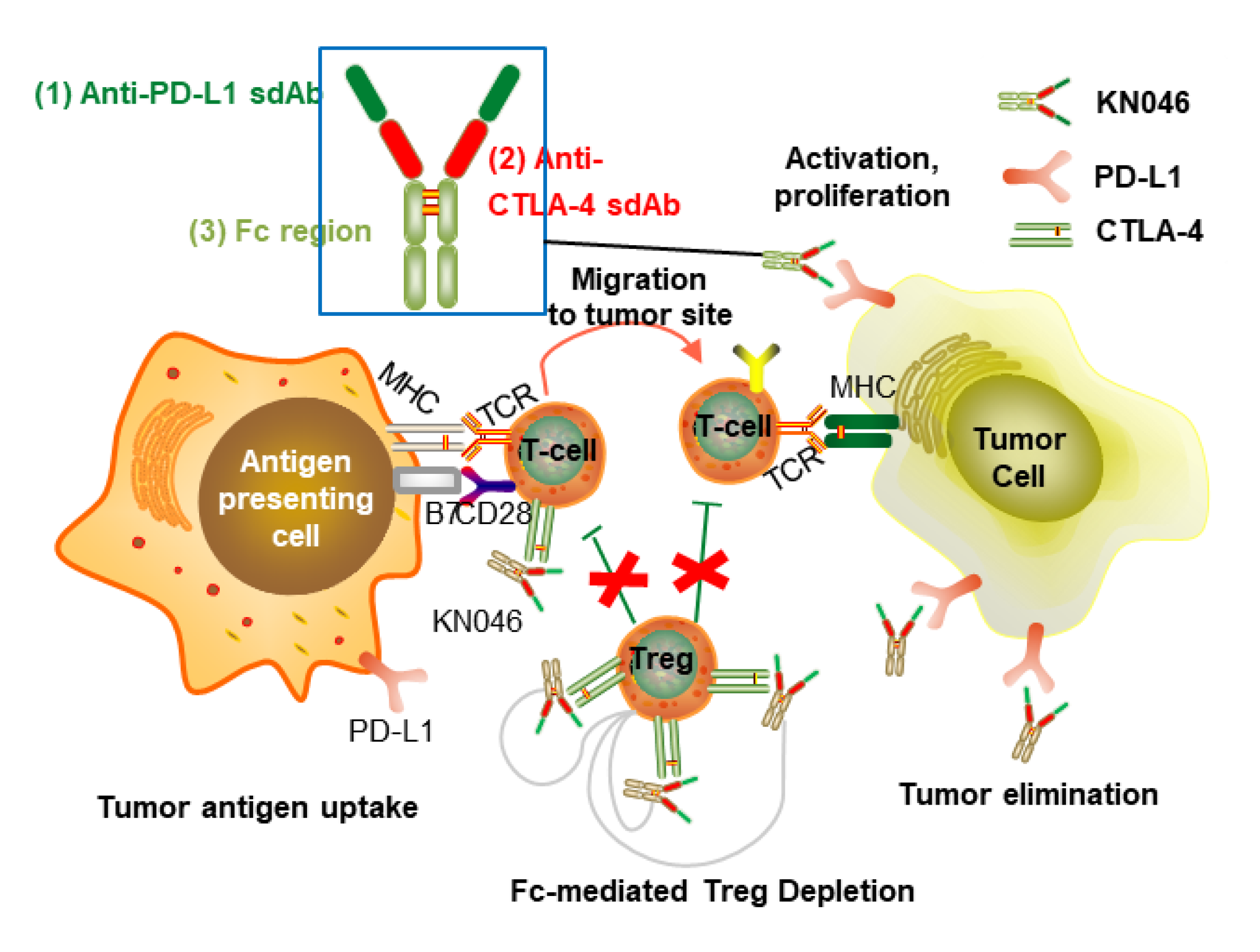
KN046жҳҜеә·е®Ғжқ°з‘һиҮӘдё»з ”еҸ‘зҡ„PD-L1/CTLA-4еҸҢзү№ејӮжҖ§жҠ—дҪ“пјҢе…¶еҲӣж–°и®ҫи®ЎеҢ…жӢ¬пјҡйҮҮз”ЁжңәеҲ¶дёҚеҗҢзҡ„CTLA-4дёҺPD-L1еҚ•еҹҹжҠ—дҪ“иһҚеҗҲз»„жҲҗпјҢеҸҜйқ¶еҗ‘еҜҢйӣҶдәҺPD-L1й«ҳиЎЁиҫҫзҡ„иӮҝзҳӨеҫ®зҺҜеўғеҸҠжё…йҷӨжҠ‘еҲ¶иӮҝзҳӨе…Қз–«зҡ„TregгҖӮ

KN046 : жҷ¶дҪ“з»“жһ„
KN046еңЁжҫіеӨ§еҲ©дәҡе’ҢдёӯеӣҪе·ІејҖеұ•иҰҶзӣ–йқһе°Ҹз»ҶиғһиӮәзҷҢгҖҒиғёи…әзҷҢгҖҒиғ°и…әзҷҢгҖҒиӮқзҷҢгҖҒйЈҹз®ЎйіһзҷҢгҖҒдёүйҳҙд№іи…әзҷҢзӯү10дҪҷз§ҚиӮҝзҳӨзҡ„иҝ‘20йЎ№дёҚеҗҢйҳ¶ж®өдёҙеәҠиҜ•йӘҢпјҢиҜ•йӘҢз»“жһңжҳҫзӨәеҮәиүҜеҘҪзҡ„е®үе…ЁжҖ§е’Ңжңүж•ҲжҖ§гҖӮзҫҺеӣҪFDAеҹәдәҺеңЁжҫіеӨ§еҲ©дәҡе’ҢдёӯеӣҪеҸ–еҫ—зҡ„дёҙеәҠиҜ•йӘҢз»“жһңпјҢжү№еҮҶKN046еңЁзҫҺеӣҪзӣҙжҺҘиҝӣе…Ҙв…ЎжңҹдёҙеәҠиҜ•йӘҢгҖӮзӣ®еүҚKN046зҡ„еӣӣйЎ№жіЁеҶҢдёҙеәҠиҜ•йӘҢжӯЈеңЁиҝӣиЎҢдёӯгҖӮ
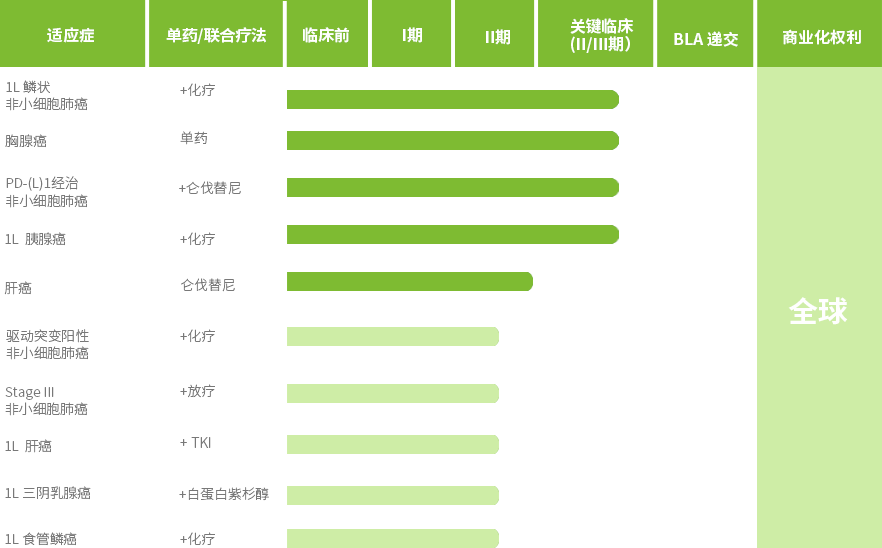
CSCO 2021 posterпјҡKN046иҒ”еҗҲзҷҪиӣӢзҷҪзҙ«жқүйҶҮ/еҗүиҘҝд»–ж»ЁдёҖзәҝжІ»з–—дёҚеҸҜеҲҮйҷӨеұҖйғЁжҷҡжңҹжҲ–иҪ¬з§»жҖ§иғ°и…әеҜјз®Ўи…әзҷҢ(PDAC)зҡ„жңүж•ҲжҖ§е’Ңе®үе…ЁжҖ§
ESMO 2021 posterпјҡKN046иҒ”еҗҲд»‘дјҗжӣҝе°јз”ЁдәҺжІ»з–—жҷҡжңҹдёҚеҸҜеҲҮйҷӨжҲ–иҪ¬з§»жҖ§иӮқз»ҶиғһзҷҢзҡ„еүҚзһ»жҖ§в…ЎжңҹдёҙеәҠиҜ•йӘҢзҡ„еҲқжӯҘз–—ж•ҲеҸҠе®үе…ЁжҖ§з»“жһң
ESMO 2021 posterпјҡKN046иҒ”еҗҲеҗ«й“ӮеҸҢиҚҜеҢ–з–—дҪңдёәжІ»з–—дјҙжңүиҖҗиҚҜжҖ§иҮҙзҷҢй©ұеҠЁеҹәеӣ зӘҒеҸҳзҡ„жҷҡжңҹйқһе°Ҹз»ҶиғһиӮәзҷҢжӮЈиҖ…зҡ„дёҖзәҝз–—жі•
ASCO 2021 posterпјҡKN046иҒ”еҗҲй“Ӯзұ»еҢ–з–—жІ»з–—жҷҡжңҹйқһе°Ҹз»ҶиғһиӮәзҷҢжӮЈиҖ…зҡ„з–—ж•ҲгҖҒе®үе…ЁжҖ§е’ҢиҖҗеҸ—жҖ§зҡ„в…ЎжңҹгҖҒејҖж”ҫгҖҒеӨҡдёӯеҝғз ”з©¶
ASCO 2021 posterпјҡKN046иҒ”еҗҲзҙ«жқүйҶҮ/йЎәй“ӮдёҖзәҝжІ»з–—дёҚеҸҜеҲҮйҷӨеұҖйғЁжҷҡжңҹгҖҒеӨҚеҸ‘жҲ–иҪ¬з§»жҖ§йЈҹз®ЎйіһзҷҢ(ESCC)зҡ„з–—ж•Ҳе’Ңе®үе…ЁжҖ§
ASCO 2021 posterпјҡKN046иҒ”еҗҲзҷҪиӣӢзҷҪзҙ«жқүйҶҮ/еҗүиҘҝд»–ж»ЁдҪңдёәдёҚеҸҜеҲҮйҷӨзҡ„еұҖйғЁжҷҡжңҹжҲ–иҪ¬з§»жҖ§иғ°и…әеҜјз®Ўи…әзҷҢ(PDAC)дёҖзәҝжІ»з–—зҡ„жңүж•ҲжҖ§е’Ңе®үе…ЁжҖ§
AACR 2021 posterпјҡKN046(PD-L1/CTLA-4еҸҢзү№ејӮжҖ§жҠ—дҪ“)иҒ”еҗҲзҷҪиӣӢзҷҪз»“еҗҲеһӢзҙ«жқүйҶҮжІ»з–—иҪ¬з§»жҖ§дёүйҳҙд№іи…әзҷҢжӮЈиҖ…зҡ„еҲқжӯҘе®үе…ЁжҖ§гҖҒиҖҗеҸ—жҖ§е’Ңз–—ж•Ҳз»“жһң
WCLC 2020 Mini oral reportпјҡKN046еңЁзҪ•и§ҒиғёйғЁиӮҝзҳӨжӮЈиҖ…дёӯзҡ„еҲқжӯҘе®үе…ЁжҖ§е’Ңжңүж•ҲжҖ§з»“жһң
WCLC 2020 posterпјҡKN046з”ЁдәҺжІ»з–—жҷҡжңҹйқһе°Ҹз»ҶиғһиӮәзҷҢ(NSCLC)жӮЈиҖ…зҡ„в…ЎжңҹдёҙеәҠз ”з©¶ж•°жҚ®
ASCO-GI 2020 posterпјҡKN046иҒ”еҗҲж”ҫеҢ–з–—жІ»з–—еӨҚеҸ‘е’ҢиҪ¬з§»жҖ§йЈҹз®ЎйіһзҷҢзҡ„еҲқжӯҘз–—ж•Ҳе’Ңе®үе…ЁжҖ§ж•°жҚ®
SITC 2020 posterпјҡKN026дёҺKN046иҒ”еҗҲжІ»з–—HER2йҳіжҖ§е®һдҪ“зҳӨжӮЈиҖ…зҡ„е®үе…ЁжҖ§гҖҒиҖҗеҸ—жҖ§е’ҢжҠ—иӮҝзҳӨжҙ»жҖ§еҲқжӯҘз»“жһң
ASCO 2020 posterпјҡKN046(PD-L1/CTLA-4еҸҢзү№ејӮжҖ§жҠ—дҪ“)еҜ№ж—ўеҫҖе…Қз–«жЈҖжҹҘзӮ№жҠ‘еҲ¶еүӮжІ»з–—ж— ж•Ҳзҡ„жӮЈиҖ…зҡ„еҲқжӯҘз–—ж•Ҳе’Ңе®үе…ЁжҖ§ж•°жҚ®
ASCO 2019 posterпјҡKN046пјҲжҠ—PD-L1/CTLA4еҸҢзү№ејӮжҖ§жҠ—дҪ“пјүйҰ–ж¬ЎдәәдҪ“иҜ•йӘҢпјҢеңЁжҷҡжңҹе®һдҪ“зҳӨдёӯе®үе…ЁжҖ§гҖҒз–—ж•Ҳе’ҢиҚҜд»ЈеҠЁеҠӣеӯҰзҡ„еҲқжӯҘз»“жһң
KN026* жҳҜеә·е®Ғжқ°з‘һйҮҮз”Ёе…·жңүиҮӘдё»зҹҘиҜҶдә§жқғFcејӮдәҢиҒҡдҪ“е№іеҸ°жҠҖжңҜ(CRIB)ејҖеҸ‘зҡ„жҠ—HER2еҸҢзү№ејӮжҖ§жҠ—дҪ“пјҢеҸҜеҗҢж—¶з»“еҗҲ HER2зҡ„дёӨдёӘйқһйҮҚеҸ иЎЁдҪҚпјҢеҜјиҮҙеҸҢHER2дҝЎеҸ·йҳ»ж–ӯпјҢиҫҫеҲ°жӣІеҰҘзҸ еҚ•жҠ—е’Ңеё•еҰҘзҸ еҚ•жҠ—иҒ”з”Ёзҡ„ж•ҲжһңпјҢеҰӮеұ•зӨәеҮәжӣҙй«ҳзҡ„дәІе’ҢеҠӣпјҢд»ҘеҸҠеңЁHER2йҳіжҖ§иӮҝзҳӨз»Ҷиғһж Әдёӯе…·еӨҮдјҳж•Ҳзҡ„иӮҝзҳӨжҠ‘еҲ¶дҪңз”ЁгҖӮеҗҢж—¶пјҢKN026еҜ№ HER2дёӯдҪҺиЎЁиҫҫиӮҝзҳӨе’ҢжӣІеҰҘзҸ еҚ•жҠ—жҠ—жҖ§з»Ҷиғһж Әд№ҹжңүжҠ‘еҲ¶дҪңз”ЁгҖӮ
 KN026 : жҷ¶дҪ“з»“жһ„
KN026 : жҷ¶дҪ“з»“жһ„KN026е·ІдәҺ2018е№ҙеҲҶеҲ«иҺ·еҫ—дёӯеӣҪеӣҪ家иҚҜе“Ғзӣ‘зқЈз®ЎзҗҶеұҖпјҲNMPAпјүе’ҢзҫҺеӣҪйЈҹе“ҒиҚҜе“Ғзӣ‘зқЈз®ЎзҗҶеұҖ(FDA)зҡ„жү№еҮҶпјҢзӣ®еүҚжӯЈеңЁдёӯеӣҪејҖеұ•еӨҡйЎ№в… /в…ЎжңҹдёҙеәҠиҜ•йӘҢпјҢеҗҢж—¶еңЁзҫҺеӣҪжҺЁиҝӣв… жңҹдёҙеәҠиҜ•йӘҢгҖӮ
в… жңҹдёҙеәҠиҜ•йӘҢз»“жһңиЎЁжҳҺпјҢKN026е…·жңүиүҜеҘҪзҡ„иҖҗеҸ—жҖ§е’Ңе®үе…ЁжҖ§пјҢеңЁеӨҡзәҝжҠ—HER2жІ»з–—еҗҺиҝӣеұ•зҡ„HER2йҳіжҖ§д№іи…әзҷҢжӮЈиҖ…дёӯиЎЁзҺ°еҮәдәҶжҳҫи‘—зҡ„жҠ—иӮҝзҳӨжҙ»жҖ§гҖӮжҷҡжңҹиғғзҷҢеҗҺзәҝзҡ„в…Ўжңҹз ”з©¶дёӯпјҢKN026еңЁHER2й«ҳиЎЁиҫҫе’ҢдёӯдҪҺиЎЁиҫҫзҡ„жӮЈиҖ…дёӯжҳҫзӨәдәҶеҲқжӯҘзҡ„з–—ж•ҲгҖӮ

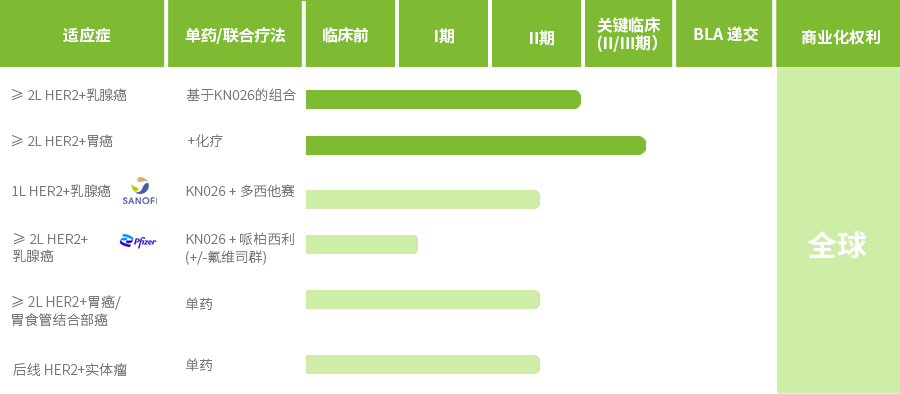
ASCO 2022 posterпјҡKN026еҗҺзәҝжІ»з–—жҷҡжңҹHER2иЎЁиҫҫзҡ„иғғзҷҢжҲ–иғғйЈҹз®Ўз»“еҗҲйғЁзҷҢзҡ„в…ЎжңҹдёҙеәҠз ”з©¶
ASCO 2021 AbstractпјҡHER2еҸҢзү№ејӮжҖ§жҠ—дҪ“KN026еңЁжҷҡжңҹHER2йҳіжҖ§иғғе’ҢиғғйЈҹз®Ўз»“еҗҲйғЁзҷҢжӮЈиҖ…дёӯзҡ„еҲқжӯҘз–—ж•Ҳ
AACR 2020 posterпјҡдҪҝз”ЁиҪ¬иҜ‘иӮҝзҳӨз”ҹй•ҝжҠ‘еҲ¶жЁЎеһӢеҸҠзҫӨдҪ“иҚҜд»ЈеҠЁеҠӣеӯҰеҲҶжһҗж–№жі•йў„жөӢHER2еҸҢзү№ејӮжҖ§жҠ—дҪ“KN026зҡ„жңүж•ҲеүӮйҮҸ
ASCO 2020 posterпјҡHER2еҸҢзү№ејӮжҖ§жҠ—дҪ“KN026еңЁHER2йҳіжҖ§иҪ¬з§»жҖ§д№іи…әзҷҢжӮЈиҖ…дёӯзҡ„еҲқжӯҘе®үе…ЁжҖ§гҖҒжңүж•ҲжҖ§е’ҢиҚҜд»ЈеҠЁеҠӣеӯҰ(PK)з»“жһң
SITC 2020 posterпјҡKN026дёҺKN046иҒ”еҗҲжІ»з–—HER2йҳіжҖ§е®һдҪ“зҳӨжӮЈиҖ…зҡ„е®үе…ЁжҖ§гҖҒиҖҗеҸ—жҖ§е’ҢжҠ—иӮҝзҳӨжҙ»жҖ§еҲқжӯҘз»“жһң
HER2йқ¶зӮ№зҡ„жІ»з–—ж•Ҳжһңдҫқиө–дәҺжңәдҪ“зҡ„йҖӮеә”жҖ§е…Қз–«еҸҚеә”пјҢеӣ жӯӨиҒ”еҗҲиӮҝзҳӨе…Қз–«зҡ„зӣёе…ійқ¶зӮ№еҰӮPD-1/PD-L1гҖҒCTLA-4зӯүеҸҜд»ҘеҚҸеҗҢеўһејәиҚҜзү©жҠ—иӮҝзҳӨзҡ„дҪңз”ЁгҖӮзӣ®еүҚHER2йқ¶еҗ‘иҚҜзү©дёҺPD-1жҠ—дҪ“иҒ”еҗҲдҪҝз”Ёе·Із»ҸеңЁHER2йҳіжҖ§зҡ„д№іи…әзҷҢе’ҢиғғзҷҢдёҠеұ•зҺ°иүҜеҘҪз–—ж•ҲпјҢеҢ…жӢ¬дёүиҒ”з–—жі•пјҲpembrolizumabгҖҒtrastuzumabе’ҢеҢ–з–—пјүеңЁHER2йҳіжҖ§иғғзҷҢе’ҢиғғйЈҹз®ЎиҝһжҺҘйғЁзҷҢзҡ„дёҖзәҝжІ»з–—ж–№жі•зҡ„еҚ•иҮӮдәҢжңҹдёҙеәҠдёӯеұ•зҺ°еҮә91%е®ўи§Ӯзј“и§ЈзҺҮпјҲORRпјү,13.0дёӘжңҲзҡ„дёӯдҪҚж— иҝӣеұ•з”ҹеӯҳжңҹпјҲPFSпјүпјҢе’Ң27.3дёӘжңҲзҡ„дёӯдҪҚжҖ»з”ҹеӯҳжңҹпјҲOSпјүгҖӮдёүиҒ”з–—жі•зҡ„дёүжңҹз ”з©¶пјҲKEYNOTE-811пјүд№ҹжӯЈеңЁиҝӣиЎҢгҖӮ
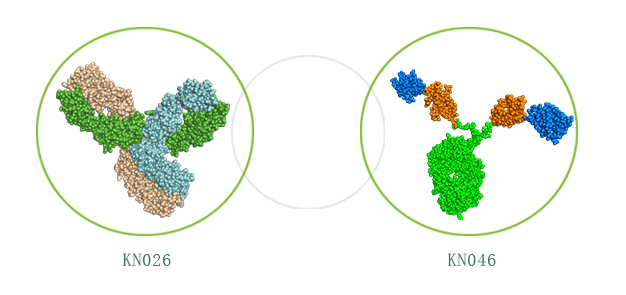
KN026е’ҢKN046дёӨз§ҚиҚҜзү©еңЁеҚ•иҚҜдёҙеәҠиҜ•йӘҢдёӯеқҮжҳҫзӨәеҮәиүҜеҘҪзҡ„е®үе…ЁжҖ§гҖҒиҖҗеҸ—жҖ§е’ҢжҠ—иӮҝзҳӨз–—ж•ҲгҖӮKN026дёҺKN046зҡ„иҒ”еҗҲз”ЁиҚҜе·Із»ҸеңЁдёҖйЎ№ејҖж”ҫгҖҒеӨҡдёӯеҝғдёҙеәҠиҜ•йӘҢдёӯй’ҲеҜ№ж ҮеҮҶжІ»з–—еӨұиҙҘзҡ„жҷҡжңҹHER2иЎЁиҫҫе®һдҪ“зҳӨжӮЈиҖ…еҸ–еҫ—дәҶеҲқжӯҘдјҳејӮз–—ж•Ҳе’Ңе®үе…ЁиҖҗеҸ—жҖ§з»“жһңгҖӮ2020е№ҙпјҢKN026дёҺKN046иҒ”еҗҲз–—жі•иҺ·зҫҺеӣҪйЈҹе“ҒиҚҜе“Ғзӣ‘зқЈз®ЎзҗҶеұҖпјҲFDAпјүжҺҲдәҲеӯӨе„ҝиҚҜиө„ж јпјҲODDпјүпјҢз”ЁдәҺжІ»з–—HER2-йҳіжҖ§жҲ–HER2-дҪҺиЎЁиҫҫиғғзҷҢеҸҠиғғйЈҹз®ЎиҝһжҺҘйғЁзҷҢпјҲGC/GEJпјүгҖӮеә·е®Ғжқ°з‘һжӯЈеңЁиҝӣиЎҢKN026иҒ”еҗҲKN046в…Ўжңҹе…ій”®жҖ§дёҙеәҠз ”з©¶(SEARCH-01)пјҢи®ЎеҲ’еңЁ20-30家дёӯеӣҪе’Ң10-20家зҫҺеӣҪдёҙеәҠз ”з©¶дёӯеҝғејҖеұ•пјҢиҜ„дј°KN026иҒ”еҗҲKN046жІ»з–—HER2йҳіжҖ§е®һдҪ“зҳӨзҡ„жңүж•ҲжҖ§гҖҒе®үе…ЁжҖ§е’ҢиҖҗеҸ—жҖ§пјҢе…¶дёӯеҢ…жӢ¬жҷҡжңҹиғғеҸҠиғғйЈҹз®Ўз»“еҗҲйғЁзҷҢзӯүгҖӮ
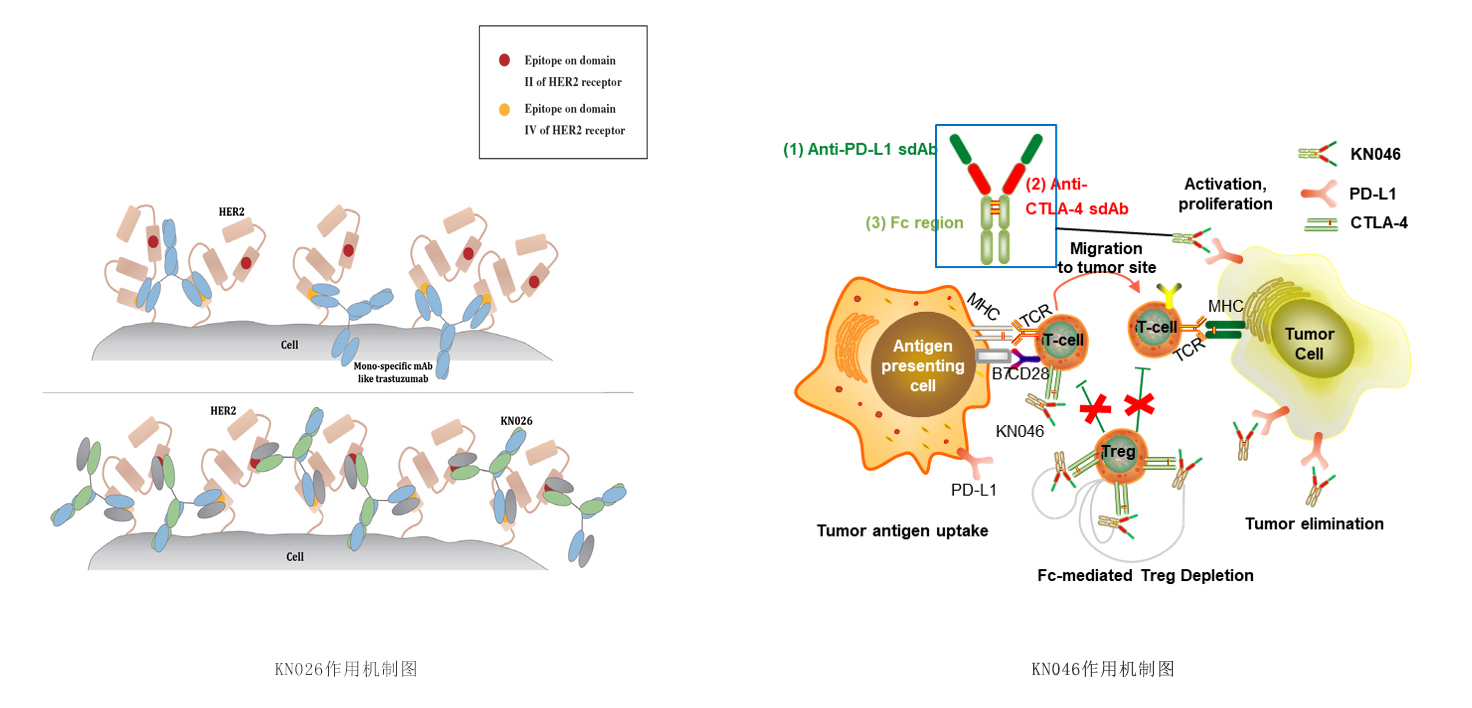

AACR 2022 posterпјҡKN046дёҺKN026иҒ”еҗҲжІ»з–—еұҖйғЁжҷҡжңҹдёҚеҸҜеҲҮйҷӨжҲ–иҪ¬з§»жҖ§HER2йҳіжҖ§е®һдҪ“зҳӨжӮЈиҖ…зҡ„еҲқжӯҘе®үе…ЁжҖ§е’Ңз–—ж•Ҳз»“жһң
SABCS 2021 posterпјҡKN026иҒ”еҗҲKN046жІ»з–—иҪ¬з§»жҖ§HER2йҳіжҖ§д№іи…әзҷҢжӮЈиҖ…зҡ„еҲқжӯҘе®үе…ЁжҖ§е’Ңз–—ж•Ҳз»“жһңпјҡдёҖйЎ№в…ЎжңҹиҜ•йӘҢ
ESMO 2021 posterпјҡKN026иҒ”еҗҲKN046з”ЁдәҺжІ»з–—HER2йҳіжҖ§ж¶ҲеҢ–йҒ“иӮҝзҳӨжӮЈиҖ…зҡ„еҲқжӯҘз–—ж•ҲеҸҠе®үе…ЁжҖ§з»“жһң
SITC 2020 poster:KN026дёҺKN046иҒ”еҗҲжІ»з–—HER2йҳіжҖ§е®һдҪ“зҳӨжӮЈиҖ…зҡ„е®үе…ЁжҖ§гҖҒиҖҗеҸ—жҖ§е’ҢжҠ—иӮҝзҳӨжҙ»жҖ§еҲқжӯҘз»“жһң
KN019дёҺиҙқжӢүиҘҝжҷ®(BelataceptпјҢиӢұж–Үе•Ҷе“ҒеҗҚпјҡNulojixВ®)зӣёеҗҢзҡ„ж°Ёеҹәй…ёеәҸеҲ—пјҢжҜ”иҮӘдҪ“е…Қз–«з–ҫз—…зҡ„йҮҚзЈ…иҚҜзү©Orenciaжҙ»жҖ§ејә10еҖҚпјҢдё”е®үе…ЁжҖ§иүҜеҘҪгҖӮKN019е·ІиҺ·еҫ—еӣҪ家иҚҜе“Ғзӣ‘зқЈз®ЎзҗҶеұҖйўҒеҸ‘зҡ„дёҙеәҠжү№д»¶гҖӮжҲӘиҮізӣ®еүҚпјҢKN019зҡ„IжңҹдёҙеәҠиҜ•йӘҢе·Із»Ҹз»“жқҹпјҢв…ЎжңҹдёҙеәҠиҜ•йӘҢжӯЈеңЁиҝӣиЎҢдёӯпјҢејҖеҸ‘з”ЁдәҺиӮҫ移жӨҚжҺ’ж–ҘеҸҚеә”е’Ңзұ»йЈҺж№ҝе…іиҠӮзӮҺзӯүиҮӘиә«е…Қз–«жҖ§йҖӮеә”з—Үзҡ„йў„йҳІдёҺжІ»з–—гҖӮеә·е®Ғжқ°з‘һиҝҳи®ЎеҲ’з ”з©¶KN019йҷҚдҪҺиӮҝзҳӨе…Қз–«еёҰжқҘзҡ„еүҜдҪңз”Ёж–№йқўзҡ„дёҙеәҠеә”з”ЁгҖӮ
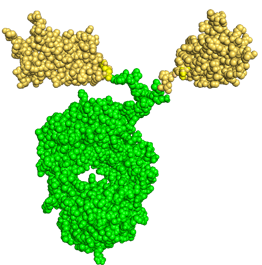 KN019 : жҷ¶дҪ“з»“жһ„
KN019 : жҷ¶дҪ“з»“жһ„
иҙқжӢүиҘҝжҷ®жҳҜдёҖз§Қе·ІиҺ·жү№дёҠеёӮзҡ„е…Қз–«жҠ‘еҲ¶еүӮпјҢз”ЁдәҺжҲҗе№ҙжӮЈиҖ…йў„йҳІиӮҫи„Ҹ移жӨҚжҺ’ж–ҘеҸҚеә”гҖӮиҙқжӢүиҘҝжҷ®зҡ„дјҳи¶Ҡз–—ж•Ҳе·ІеңЁдёҙеәҠиҜ•йӘҢзҡ„й•ҝжңҹи·ҹиёӘз ”з©¶дёӯеҫ—еҲ°дәҶе……еҲҶзҡ„иҜҒе®һгҖӮ
иҙқжӢүиҘҝжҷ®жҳҜеҹәдәҺйҳҝе·ҙиҘҝжҷ®пјҲAbataceptпјҢиӢұж–Үе•Ҷе“ҒеҗҚпјҡ OrenciaВ®)иҝӣиЎҢж”№иҝӣзҡ„иҚҜзү©пјҢе…¶иҚҜж•ҲжӣҙејәгҖӮ йҳҝе·ҙиҘҝжҷ®иў«жү№еҮҶз”ЁдәҺзұ»йЈҺж№ҝжҖ§е…іиҠӮзӮҺгҖҒзү№еҸ‘жҖ§е…іиҠӮзӮҺе’Ңзүӣзҡ®зҷЈе…іиҠӮзӮҺзҡ„жІ»з–—пјҢ2017е№ҙйҳҝе·ҙиҘҝжҷ®зҡ„е…Ёзҗғй”Җе”®йўқзәҰдёә27дәҝзҫҺе…ғгҖӮ

иҙқжӢүиҘҝжҷ®зҡ„иӣӢзҷҪиҙЁз»“жһ„е…·жңүеӨҚжқӮзҡ„дёҺеҠҹиғҪзӣёе…ізҡ„зі–еҹәеҢ–гҖӮеҲ°зӣ®еүҚдёәжӯўпјҢе…ЁзҗғиҝҳжІЎжңүе…¶д»–е…¬еҸёиғҪеӨҹејҖеҸ‘еҮәиҙқжӢүиҘҝжҷ®з”ҹзү©зұ»дјјиҚҜгҖӮKN019з”ҹдә§еҫ—зҺҮй«ҳпјҢиӣӢзҷҪзҡ„дёҖзә§з»“жһ„гҖҒй«ҳзә§з»“жһ„е’Ңзҝ»иҜ‘еҗҺдҝ®йҘ°дёҺеҺҹз ”иҚҜй«ҳеәҰзӣёдјјпјҢиҚҜзҗҶжҜ’зҗҶз ”з©¶з»“жһңд№ҹдёҺеҺҹз ”иҚҜй«ҳеәҰдёҖиҮҙпјҢеӣ жӯӨжңүжңӣжҲҗдёәиҙқжӢүиҘҝжҷ®зҡ„йҰ–дёӘз”ҹзү©зұ»дјјиҚҜгҖӮеҗҢж—¶пјҢжҲ‘们д№ҹдјҡж”№иүҜеҲ¶еүӮпјҢз”ЁдәҺеӨҡдёӘе…Ёж–°йҖӮеә”з—Үзҡ„дёҙеәҠејҖеҸ‘гҖӮ

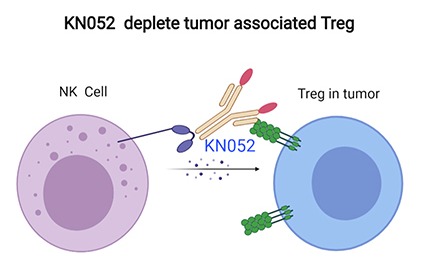
KN052жҳҜеә·е®Ғжқ°з‘һеҲ©з”Ёе…¬еҸёеҸҢжҠ—е№іеҸ°жҠҖжңҜиҮӘдё»з ”еҸ‘зҡ„PD-L1/OX40еҸҢзү№ејӮжҖ§жҠ—дҪ“пјҢиғҪеӨҹеҗҢж—¶иҜҶеҲ«PD-L1дёҺOX40пјҢеҸҜжңүж•Ҳйҳ»ж–ӯPD-L1дёҺPD-1зҡ„зӣёдә’дҪңз”ЁпјҢ并жҝҖжҙ»OX40дҝЎеҸ·йҖҡи·ҜгҖӮдёҖж–№йқўйҳ»жӯўиӮҝзҳӨз»Ҷиғһзҡ„“е…Қз–«йҖғйҖё”пјҢеҸҰдёҖж–№йқўеўһејәTз»Ҷиғһзҡ„жҙ»еҢ–пјҢ并еҮҸе°‘Tregд»ӢеҜјзҡ„е…Қз–«жҠ‘еҲ¶пјҢеҚҸеҗҢеўһејәжҠ—иӮҝзҳӨжҙ»жҖ§гҖӮ
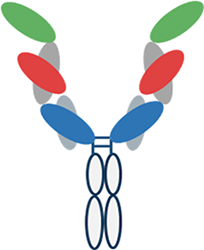
KN052 : еҲҶеӯҗз»“жһ„
PD-L1жӢ®жҠ—еүӮе’ҢOX40жҝҖеҠЁеүӮеңЁеҗҢдёҖеҲҶеӯҗдёӯдә§з”ҹжҙ»жҖ§пјӣжӯӨдёІиҒ”з»“жһ„з”ЁдәҺжҠ—еҺҹз»“еҗҲз»“жһ„еҹҹжҺ’еҲ—д»ҘеҮҸејұжҠ—OX40жҜ’жҖ§пјӣдҝқз•ҷе®Ңж•ҙFcеҠҹиғҪзҡ„йҮҺз”ҹеһӢIgG1 FcпјӣOX40жҳҜдёҖзұ»е…ій”®зҡ„Tз»Ҷиғһе…ұеҲәжҝҖеҲҶеӯҗпјҢOX40е’ҢOX40Lз»“еҗҲеўһеҠ ж•Ҳеә”Tз»Ҷиғһе’Ңи®°еҝҶTз»Ҷиғһзҡ„еӯҳжҙ»е’Ңжү©еўһпјҢеўһеҠ з»Ҷиғһеӣ еӯҗзҡ„еҲҶжіҢпјӣеҸҜдҪңдёәдҪҗеүӮдёҺиӮҝзҳӨз–«иӢ—е’Ңз»ҶиғһжІ»з–—иҒ”еҗҲдҪҝз”ЁгҖӮ
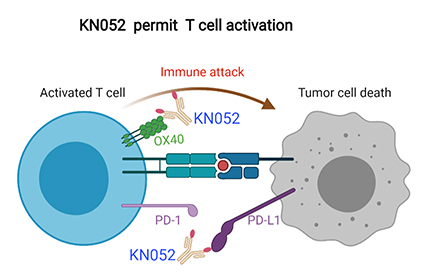
дёҙеәҠеүҚз ”з©¶дёӯпјҢKN052зҡ„жҙ»жҖ§жҳҺжҳҫејәдәҺдёӨдёӘеҚ•йқ¶зӮ№еҜ№з…§жҠ—дҪ“еҚ•з”ЁеҸҠиҒ”з”ЁгҖӮ2022е№ҙ2жңҲпјҢKN052зҡ„ж–°иҚҜдёҙеәҠиҜ•йӘҢз”іиҜ·пјҲINDпјүиҺ·еҫ—дёӯеӣҪеӣҪ家иҚҜе“Ғзӣ‘зқЈз®ЎзҗҶеұҖпјҲNMPAпјүжү№еҮҶпјҢеңЁдёӯеӣҪејҖеұ•в… жңҹдёҙеәҠз ”з©¶гҖӮ2022е№ҙ6жңҲпјҢв… жңҹдёҙеәҠз ”з©¶пјҲKN052-CHN-001пјүе®ҢжҲҗйҰ–дҫӢжӮЈиҖ…з»ҷиҚҜгҖӮ